Valproate (Dépakine): Le Canard Enchaîné jette un vif débat

Last Updated on octobre 2, 2016 by Joseph Gut – thasso
05 septembre 2016 – Cette histoire par Vincent Bargoin a été publié titré “Dépakine: une étude «alarmante» cachée aux familles selon le Canard, le Ministère dément” au Medscape Francais et ce reflète en essence dans leur formulation si dessous.
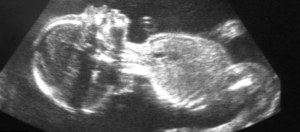 PARIS, FRANCE – Dans un article publié en date du 10 août 2016, le Canard Enchaîné revient sur l’affaire de la Dépakine en citant un rapport montrant que plus de 10 000 femmes enceintes ont pris l’anti-épileptique entre 2007 et 2014 alors que les dangers de malformations pour les enfants à naître étaient déjà connus. Le journal satirique dénonce une étude “alarmante” (menée conjointement par l’agence du médicament ANSM et la Caisse nationale d’assurance maladie) qui sous-tend que les victimes de malformations devraient donc se compter par milliers, laquelle aurait été communiquée au ministère de la Santé “dès la mi-juillet”, mais “soigneusement cachée aux familles”. Sans s’exprimer sur la véracité des chiffres, le Ministère des Affaires sociales et de la Santé se défend ce jour, dans un communiqué, d’un manque de transparence. Il “dément plusieurs informations publiées dans l’édition du Canard Enchaîné” et précise que “contrairement à ce qui est affirmé, l’étude réalisée par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) et la Caisse nationale d’assurance maladie (CNAMTS) n’est pas cachée aux familles” et qu’une présentation du premier volet [de l’étude en question] par le Directeur général de la santé à l’association d’Aide aux Parents d’Enfants souffrant du Syndrome de l’Anti-Convulsivant (APESAC) est bien prévue le 24 août.
PARIS, FRANCE – Dans un article publié en date du 10 août 2016, le Canard Enchaîné revient sur l’affaire de la Dépakine en citant un rapport montrant que plus de 10 000 femmes enceintes ont pris l’anti-épileptique entre 2007 et 2014 alors que les dangers de malformations pour les enfants à naître étaient déjà connus. Le journal satirique dénonce une étude “alarmante” (menée conjointement par l’agence du médicament ANSM et la Caisse nationale d’assurance maladie) qui sous-tend que les victimes de malformations devraient donc se compter par milliers, laquelle aurait été communiquée au ministère de la Santé “dès la mi-juillet”, mais “soigneusement cachée aux familles”. Sans s’exprimer sur la véracité des chiffres, le Ministère des Affaires sociales et de la Santé se défend ce jour, dans un communiqué, d’un manque de transparence. Il “dément plusieurs informations publiées dans l’édition du Canard Enchaîné” et précise que “contrairement à ce qui est affirmé, l’étude réalisée par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) et la Caisse nationale d’assurance maladie (CNAMTS) n’est pas cachée aux familles” et qu’une présentation du premier volet [de l’étude en question] par le Directeur général de la santé à l’association d’Aide aux Parents d’Enfants souffrant du Syndrome de l’Anti-Convulsivant (APESAC) est bien prévue le 24 août.
Rappelons que les risques associés à l’utilisation de Dépakine® pendant la grossesse sont établis ainsi que le rappelait le Pr Sophie Dupont, neurologue épileptologue à l’Hôpital de la Pitié-Salpêtrière dans une interview pour Medscape : “Depuis les années 80, on savait que la Dépakine® augmentait le risque de spina bifida. Des données de 2013 ont montré que le risque de malformations des enfants exposés in utero était majoré de 11% à la naissance (anomalies du tube neural et fente palatine) comparé à un risque de 2 à 3 % dans la population générale. On sait aussi que le taux de malformations est fortement dose-dépendant. Les troubles neurodéveloppementaux notamment les retards de QI (10 points en moins) et le risque accru d’autisme ont été mis en évidence plus récemment. Les nouvelles données confirment que les enfants exposés in utero présentent un risque accru de troubles neurodéveloppementaux certainement dépendants de la dose là-encore. En parallèle, le risque de trouble du spectre autistique serait triplé et celui de l’autisme de la petite enfance quintuplé”.
Pour ce qui des chiffres, l’Inspection générale des affaires sociales (voir article ci-dessous) faisait état en février dernier de 450 naissances d’enfants exposés in utero au valproate et porteurs de malformations congénitales. L’Igas pointait alors un clair “manque de réactivité” des autorités sanitaires françaises.
450 cas de malformations sous Dépakine: l’Igas dénonce l’inertie des autorités sanitaires
Le 24 février 2016, l’Inspection Générale des Affaires Sociales (Igas) vient de rendre un rapport commandé le 22 juin 2015 par le Ministère de la Santé, sur les conséquences de la prise de valproate de sodium (Dépakine®, Dépakote®, Dépamide®, Micropakine® et génériques) par des femmes enceintes. Même s’il souligne que l’antiépileptique est parfois sans alternative, le rapport est très sévère sur le manque de réactivité des autorités sanitaires face à des risques qui, au début des années 80, étaient déjà fortement suspectés, et qui au début des années 2000, étaient avérés.
“On peut considérer qu’en 2004, l’accumulation des signaux justifiait des mesures d’information à l’attention des prescripteurs et des patients” souligne le rapport, en ajoutant que dans la notice destinée aux patients, “l’explicitation des risques liés à une grossesse sous traitement au valproate de sodium n’intervient qu’en 2010”. Auparavant, un simple renvoi du type “Consulter votre médecin en cas de grossesse, était notifié”.
450 enfants victimes de malformations
Le rapport de l’Igas est essentiellement consacré à l’avancée des connaissances scientifiques sur le valproate, et au retard dans la prise en compte de ces connaissances. Il comporte également une évaluation de l’impact de la prise de valproate par des femmes enceintes, en termes de malformations infantiles. En France, pour la période 2006-2014, les experts de l’Igas avancent un chiffre compris entre 425 et 450 cas de naissances d’enfants vivants ou mort-nés, exposés in utero au valproate et porteurs de malformations congénitales.
Ce chiffre est une extrapolation des données du registre des malformations en Rhône-Alpes (REMERA), qui a extrait tous les cas d’enfants nés vivants ou non entre 2006 et 2014, et exposés au valproate. Au total, 33 enfants exposés ont été identifiés. Pour 29 d’entre eux, la mère était traitée pour épilepsie, et pour les 4 autres, pour raisons psychiatriques. Enfin, on compte 22 naissances vivantes, et 11 interruptions médicales de grossesse.
Dans son rapport, l’Igas distingue trois périodes.
De 1967 à 2000, année où les premiers résultats des enquêtes sont discutés dans un cadre européen. En France, les premiers RCP et notices datent de 1986, et ne subissent aucun changement jusqu’en 1995. En 1997, la notion de polymalformations et de dysmorphie faciale est ajoutée. Toutefois, si les risques tératogènes sont évoqués, les RCP soulignent par ailleurs que ni leur “réalité”, ni leur “fréquence” ne sont établies. Ce doute explicite sur la réalité du risque ne sera retiré qu’en 2000. La notice destinée aux patients, elle, dans sa version 1997, recommande simplement de “consulter rapidement votre médecin en cas de grossesses ou de désir de grossesse” – sans davantage d’information sur la nature du risque.
Entre contraception et conception, rien qu’un lapsus
En page 35, le rapport de l’Igas rapporte cette très belle histoire. Jusqu’en 1995, le RCP signalait que “en cas de grossesse, il n’est pas légitime de déconseiller une conception”. On peut s’interroger sur cette formulation, puisque si grossesse il y a, conception il y a eu. En 1995, la formule devient : “en cas de grossesse, il n’est pas légitime de déconseiller une contraception”. La formule ne se comprend guère mieux. Mais surtout, le rapport de l’Igas révèle que la formulation initiale a été rétablie en 1997, “révélant que l’inversion du message n’était pas intentionnelle”. Ce qu’au demeurant, l’ANSM a confirmé, évoquant pour sa part “une erreur rédactionnelle”.
Seconde période : 2001-2006, années durant lesquelles “le risque malformatif est avéré, et le retard neurodéveloppemental, débattu”. Un rapport britannique de 2002, puis un rapport suédois de 2003 sur le risque de tératogénicité, aboutissent en févier 2004 à la proposition d’une mention commune, européenne (qui n’évoque pas encore retard le retard de développement). En France, la modification des RCP ne sera effective qu’en 2006. Le valproate devient déconseillé aux femmes en âge de procréer, chez lesquelles il convient d’adopter des alternatives thérapeutiques, dans la mesure du possible. Le rapport de l’Igas précise que les notices britannique, allemande, belge et irlandaise des années 2002, 2003, et 2004, ont pu être consultées. Elles précisaient les risques malformatifs et comportaient des informations détaillés, notamment sur le défaut de fermeture du tube neural. D’où cette litote : “Dans une approche comparative, la France n’est pas au nombre des pays les plus réactifs”.
Et aux Etats-Unis ?
En 2009, la FDA publie un communiqué alertant les professionnels de santé sur les effets tératogènes du valproate, la nécessité d’informer les patientes des risques potentiels, et la nécessité d’envisager des alternatives thérapeutiques. En 2011, l’agence américaine récidive en ces termes : “la FDA informe le public que les enfants nés de mère sous valproate de sodium ou produit apparenté durant la grossesse, présentent un risque accru de retards cognitifs comparés aux enfants exposés à d’autres antiépileptiques durant la grossesse”.
Enfin, la période 2006-2014, qui se conclut par une prise de position commune aux états européens sur les mesures de minimisation des risques. Dans une approche comparative, la France n’est pas au nombre des pays les plus réactifs. La France rattrape alors son retard, puisque selon une enquête menée par l’EMA en 2012, elle fait dorénavant partie des quelques pays européens qui mentionne, outre les risques tératogènes, l’autisme et les retards de QI dans les RCP. Faut-il voir là l’effet Médiator ?
ET AUJOURD’HUI?
L’interdiction du valproate de sodium était et reste une décision quasi impossible à prendre. « Les maladies chroniques traitées par ce médicament présentent également des risques graves pour la mère et le fœtus “rappellent d’ailleurs les experts de l’Igas dès l’introduction du rapport.
C’est sans doute un peu moins vrai dans le cas des troubles bipolaires:”le caractère indispensable du valproate pour certaines patientes, qui ne fait pas débat en matière d’épilepsie, gagnerait à être réexaminé en psychiatrie”. Mais *dans le cas de l’épilepsie un arrêt ou un changement de traitement brutal peut avoir des conséquences graves, voire mortelles pour la mère et pour l’enfant”.
Et d’ajouter que “l’éviction systématique du valproate de sodium ne peut être envisagé que dans le cadre de stratégies thérapeutiques qui doivent s’appuyer sur l’existence de traitements alternatifs et sur une analyse des bénéfices et des risques”.
Néanmoins, a-t-on véritablement donné aux médecins – et aux patientes – les moyens de peser ce rapport bénéfice/risque ? Les experts de l’Igas soulignent “des retards dans la prise en compte des données acquises de la science, notamment dans les années 90, ou l’intégralité des malformations n’est pas renseignée, et au début des années 2000, où les risques de retard de développement ne sont pas mentionnés. Dans plusieurs pays européens, ces risques sont évoqués dès 2003-2004, alors qu’il faut attendre 2006 en France”. Et de pointer “des divergences d’information entre différentes spécialités contenant du valproate de sodium, notamment entre les médicaments princeps et les génériques, ces derniers ne bénéficiant d’une information actualisée que depuis juin 2015”.
Au total, “le constat de la mission est celui d’un manque de réactivité des autorités sanitaires et du principal titulaire de l’AMM. Les alertes ont été, au plan français et au plan européen, motivé davantage par des signaux exogènes, notamment médiatiques, que par une prise en compte des données de pharmacovigilance et des publications scientifiques”.
Brève histoire du valproate
La molécule commence sa carrière en 1967 (sous le nom d’Eurekene®). Initialement commercialisée par laboratoire J. Berthier, puis Berthier-Derol, cédée au laboratoire Labaz en 1981, elle sera reprise par Sanofi en 1994.
Les alertes ont été, au plan français et au plan européen, motivé davantage par des signaux exogènes, notamment médiatiques, que par une prise en compte des données de pharmacovigilance et des publications scientifiques.
Le valproate se montre rapidement précieux dans le traitement de l’épilepsie, et reste aujourd’hui un traitement de référence. Depuis 1977, il est également largement prescrit en psychiatrie, comme traitement des troubles bipolaires, comme alternative au lithium.
L’analyse de la littérature montre que les premiers signaux de sécurité remontent à plus de 30 ans. “Les premières alertes sur le caractère tératogène des traitements antiépileptiques en général apparaissent au début des années 80”, indique le rapport de l’Igas. Parallèlement, “le risque spécifique de malformations congénitales liées à l’exposition in utero au valproate de sodium se confirme progressivement à partir des années 80”.
On relève en particulier une grande étude de cohorte rétrospective menée en 1999 (SAMREN), qui “apporte la preuve d’une relation dose-effet [tératogènes] significative pour le valproate”. Et l’année suivante, l’étude MADRE permet d’identifier et de quantifier les risques spécifiques de malformations congénitales associées aux principaux antiépileptiques.
Il faudra cependant attendre la fin des années 2000 pour que “les résultats des études prospectives [permettent] d’attribuer avec certitude au valproate des effets délétères sur le développement cognitif et comportemental des enfants exposés in utero”.
Dernière observation en date : la relation, définitivement prouvée en 2013, entre l’exposition au valproate et une forme d’autisme.
Comme c’est souvent le cas en matière d’anomalie congénitale par exposition à un toxique, la compréhension de la physiopathologie de l’exposition in utero au valproate reste “incomplète”. Certaines observations suggérant un risque accru si un frère ou une sœur, non exposé, a développé un trouble neurodéveloppemental, la notion d’une susceptibilité génétique est évoquée. L’hypothèse d’un risque associé au traitement du père est également soulevée. L’Igas signale une synthèse des connaissances disponibles sur le site du Centre de référence sur les agents tératogènes.
REFERENCE :
- Chastel X, Essid A, Lesteven P. Enquête relative aux spécialités pharmaceutiques contenant du valproate de sodium. Rapport Igas n°2015-094R, publié le 23 février 2016.
Voilà aussi les informations actuelles venant de l’ANSM sur le sujet: <http://ansm.sante.fr/Dossiers/Valproate-et-derives/Valproate-et-derives/(offset)/0>







0 Commentaire sur «Valproate (Dépakine): Le Canard Enchaîné jette un vif débat»