Variantes genómicas rastreadas hasta trastornos genéticos: ¿un nuevo enfoque?
Last Updated on enero 16, 2023 by Joseph Gut – thasso
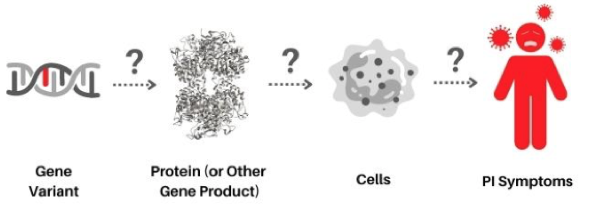
15 de enero de 2023 – En la medicina de precisión y/o dirigida de hoy en día, los médicos generalmente comienzan con la determinación de la expresión fenotípica de una enfermedad del paciente (es decir, establecen un hallazgo clínico) y luego continúan descubriendo los antecedentes genéticos del paciente ( es decir, variaciones genéticas en el mismo) que pueden ser responsables (en la base) del fenotipo del paciente/enfermedad identificado. Esta sería la vía de investigación actual de “fenotipo a genotipo”. Sin embargo, es imaginable invertir este camino y generar un camino de “genotipo a fenotipo” en su lugar. Por lo tanto, en tal enfoque, uno podría rastrear  con éxito las variantes genómicas hasta los trastornos genéticos en los pacientes. Este concepto posiblemente cambiaría la medicina reactiva por la medicina proactiva/preventiva.
con éxito las variantes genómicas hasta los trastornos genéticos en los pacientes. Este concepto posiblemente cambiaría la medicina reactiva por la medicina proactiva/preventiva.
De hecho, en esta línea, investigadores de los Institutos Nacionales de Salud (NIH) de EE. UU. acaban de publicar una evaluación de 13 estudios que adoptaron el llamado enfoque de “primero el genotipo” para la atención al paciente, lo que en sí mismo supondría una revolución en la medicina de todos los días. En estos estudios, se seleccionaron pacientes con variantes genómicas específicas y luego se estudiaron sus rasgos y síntomas. Los hallazgos descubrieron nuevas relaciones entre los genes de los pacientes y las condiciones clínicas, ampliaron los rasgos y los síntomas asociados con los trastornos conocidos y ofrecieron información sobre los trastornos recién descritos.
El presente estudio en el American Journal of Human Genetics demostró que la investigación del “primero el genotipo” es útil, especialmente para identificar a las personas con trastornos raros que de otro modo no habrían recibido atención clínica, según el Dr. Wilczewski de National Human Genome Research Institut (NHGRI) y primer autor. El estudio publicado documenta tres tipos de descubrimientos desde un enfoque de “primero el genotipo”. En  primer lugar, este enfoque ayudó a los investigadores a descubrir nuevas relaciones entre las variantes genómicas y los rasgos clínicos específicos. Por ejemplo, tener más de dos copias del gen TPSAB1 se asoció con síntomas relacionados con el tracto gastrointestinal, los tejidos conectivos y el sistema nervioso. En segundo lugar, este enfoque ayudó a los investigadores a encontrar síntomas novedosos relacionados con un trastorno que los médicos habían pasado por alto anteriormente porque el paciente no tenía los síntomas típicos. Los investigadores del NHGRI identificaron a una persona con una variante genómica asociada con un trastorno metabólico conocido. Pruebas adicionales encontraron que el individuo tenía altos niveles de ciertas sustancias químicas en su cuerpo asociadas con el trastorno, a pesar de tener solo síntomas menores. En tercer lugar, este enfoque permitió a los investigadores determinar la función de variantes genómicas específicas, lo que tiene el potencial de ayudar a los médicos a comprender los trastornos recién descritos. Por ejemplo, en un estudio, los investigadores del NHGRI y sus colaboradores encontraron que una variante genómica estaba asociada con una disfunción inmunitaria a nivel molecular en las células sanguíneas.
primer lugar, este enfoque ayudó a los investigadores a descubrir nuevas relaciones entre las variantes genómicas y los rasgos clínicos específicos. Por ejemplo, tener más de dos copias del gen TPSAB1 se asoció con síntomas relacionados con el tracto gastrointestinal, los tejidos conectivos y el sistema nervioso. En segundo lugar, este enfoque ayudó a los investigadores a encontrar síntomas novedosos relacionados con un trastorno que los médicos habían pasado por alto anteriormente porque el paciente no tenía los síntomas típicos. Los investigadores del NHGRI identificaron a una persona con una variante genómica asociada con un trastorno metabólico conocido. Pruebas adicionales encontraron que el individuo tenía altos niveles de ciertas sustancias químicas en su cuerpo asociadas con el trastorno, a pesar de tener solo síntomas menores. En tercer lugar, este enfoque permitió a los investigadores determinar la función de variantes genómicas específicas, lo que tiene el potencial de ayudar a los médicos a comprender los trastornos recién descritos. Por ejemplo, en un estudio, los investigadores del NHGRI y sus colaboradores encontraron que una variante genómica estaba asociada con una disfunción inmunitaria a nivel molecular en las células sanguíneas.
Estos resultados indican que en un concepto de “primero el genotipo”, podría ser posible explotar y conocer el espectro completo de síntomas y enfermedades (manifiestos y raros) de los que las variantes genómicas pueden ser responsables. Dado el hecho de que los genes (o sus variantes alélicas) y sus proteínas codificadas normalmente están involucrados en un número ilimitado de vías biológicas, un amplio espectro de síntomas resultantes o fenotipos clínicos que incluso se originan a partir de una sola variación genética no debería ser demasiado sorprendente e incluso debería esperarse.
Primero el genotipo
Sin embargo, para convertirse en un estándar aceptado en la medicina predictiva aplicada, el estudio también ilustra las limitaciones que habría que superar. Por lo tanto, los 13 estudios que implementaron un enfoque de genotipo primero utilizaron datos genómicos del Reverse Phenotyping Core de NHGRI en el Center for Precision Health Research. El núcleo agrega datos genómicos de programas como ClinSeq(R) y el Protocolo de secuenciación centralizada del Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAID), que juntos permitieron realizar análisis en más de 16 000 participantes de investigación que se han sometido a la  secuenciación del genoma o del exoma. Todos estos pacientes/participantes del estudio dieron su consentimiento para un amplio intercambio de datos genómicos y para ser contactados nuevamente para futuras investigaciones. Para que el “primero el genotipo” sea un medio verdaderamente aceptado y productivo de medicina predictiva (es decir, tanto para pacientes como para médicos), tendrían que cumplirse algunas condiciones.
secuenciación del genoma o del exoma. Todos estos pacientes/participantes del estudio dieron su consentimiento para un amplio intercambio de datos genómicos y para ser contactados nuevamente para futuras investigaciones. Para que el “primero el genotipo” sea un medio verdaderamente aceptado y productivo de medicina predictiva (es decir, tanto para pacientes como para médicos), tendrían que cumplirse algunas condiciones.
Primero, los marcos de datos y los centros centrales tendrían que abrirse a las comunidades médicas y de pacientes y proporcionar un amplio intercambio de datos genómicos y fenotípicos con la capacidad de volver a contactar a los participantes declarados explícitamente durante el proceso de consentimiento informado. Estos centros y sus procesos tendrían que ser validados, aprobados y bajo control de las autoridades sanitarias nacionales.
En segundo lugar, los procesos de consentimiento personal y el intercambio de datos genómicos y fenotípicos personales también tendrían que estar bajo la aprobación de las autoridades sanitarias. Esto en combinación con una implementación extremadamente estricta de los controles de privacidad. El recontacto y el rastreo de personas/pacientes sería un tema muy delicado en este contexto y necesitaría una regulación muy estricta.
En tercer lugar, cada vez más individuos/pacientes obtienen datos de análisis de secuenciación de ADN o genoma completo (pruebas genéticas directas al consumidor) por una variedad de razones. Estos datos individuales pueden contener información invaluable de variantes genéticas potencialmente iniciadoras de enfermedades de las que el individuo en particular es portador, pero no pueden reconocerlas de manera predictiva, porque todavía no hay ningún síntoma fenotípico. Los marcos de datos y los centros centrales deberán ser capaces de integrar dichos datos genéticos de pacientes individuales en sus marcos (nuevamente bajo los más altos estándares de privacidad) para encontrar en un análisis comparativo a mayor escala alelos de riesgo genético ocultos o raros, que pueden o no afectar el portador actual o en el futuro de una enfermedad manifiesta o rara (es decir, producir un fenotipo clínico).
Por último, a nivel legal y de seguros de salud/o de vida, se deben desarrollar regulaciones para manejar los riesgos prospectivos basados en el genoma en la salud y/o la enfermedad, que pueden ser reconocidos en una gran base de población pero que pueden o nunca. materializarse sobre la base de un solo individuo. Ser portador no lo convierte en culpable ni en una víctima real de la enfermedad.
General
Entonces, en conclusión, el nuevo enfoque de rastrear las variantes genómicas hasta los trastornos genéticos (es decir, el enfoque del genotipo primero) ciertamente tiene un gran potencial. Por el momento quizás más en el área de investigación clínica que en medicina práctica y aplicada y atención al paciente. Para convertirse en el verdadero estándar en la medicina predictiva/preventiva que prioriza el genotipo aplicada todos los días y al servicio de los médicos, los médicos tratantes y los “pacientes” por igual, aún se necesitan grandes esfuerzos. Puede ser fácil que una variante genética sea inocente hasta que se pruebe su culpabilidad.
Descargo de responsabilidad: Las imágenes y/o videos (si los hay) en este blog pueden estar protegidos por derechos de autor. Todos los derechos permanecen con el propietario de estos derechos.


Deja una respuesta
Lo siento, debes estar conectado para publicar un comentario.
Optional: Social Subscribe/Login