Teratogenität des Wirkstoffes Acitretin: Ausweitung des Kontrazeptionszeitraumes nach Therapieende auf 3 Jahre
Last Updated on September 15, 2016 by Joseph Gut – thasso
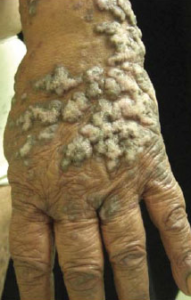
15. September 2016 – Der Wirkstoff Acitretin ist ein Retinoid, welcher zur Behandlung von schweren und schwersten Verhornungsstörungen der Haut (z.B. Psoriasis, Ichthyosis, Lichen ruber planus) in verschiedenen Ländern wie z.B. in Deutschland als Acicutan, in Österreich, Deutschland, und der Schweiz als Neotigason, und in den USA und Kanada als Soriatane zugelassen ist. Der Wirkstoff ist ein Derivat des Vitamins A.
Aufgrund des bisher schon bekannten teratogenen Risikos ist Acitretin für Frauen im gebärfähigen Alter strikt kontraindiziert, es sei denn, eine Schwangerschaft wurde vor der Therapie ausgeschlossen und es ist eine wirksame und andauernde Empfängnisverhütung während der Behandlung und nach Therapieende gewährleistet.
Das Bundesamt for Arzneimittel und Medizinprodukte (BfArM) informiert darüber, dass im Ergebnis des europäischen PSUR-Worksharing-Verfahrens für den Wirkstoff Acitretin festgelegt wurde, dass der bisherige 2-Jahres-Kontrazeptionszeitraum nach Therapieende nicht ausreichend ist und deshalb auf 3 Jahre ausgeweitet werden muss.
Alkoholkonsum kann dazu führen, dass Acitretin zu Etretinat verstoffwechselt wird, welches ebenfalls hochgradig teratogen wirkt. Etretinat lagert sich im Fettgewebe ab und hat dadurch eine sehr lange Halbwertszeit (ca. 120 Tage). Patientinnen im gebärfähigen Alter dürfen deshalb während der Therapie und 2 Monate nach Beendigung der Therapie mit Acitretin keinen Alkohol (aus Getränken, Nahrung oder Arzneimitteln) zu sich nehmen. Das Einhalten der Vorgaben bezüglich Schwangerschaftstests und Empfängnisverhütung (bis 3 Jahre nach Therapieende) bei Frauen im gebärfähigen Alter ist unbedingt erforderlich. Im weiteren dürfen Patienten innerhalb von 3 Jahren nach Beendigung einer Acitretintherapie kein Blut spenden.
Lesen sie hier weitere informationen zu Acitretin und hier zur Beurteilung der Teratogenität von weiteren Retinoid-haltigen Arzneimitteln in der Europäischen Union (EU). Insgesamt darf man hier schon festhalten, dass Arzneimittel, welche den Wirkstoff Acitretin enthalten, doch eher problematisch in ihrer sicheren Anwendung sind, in diesem Falle speziell für Frauen im gebärfähigen Alter. Im weiteren ist hier festzuhalten, dass Acitretin (Soriatane) in den USA mit einem “Boxed Warning” in seiner Fachinformation versehen ist, welches seit mindestens Mai 2015 bereits eine 3-jährige Kontrazeptionsperiode ultimativ verlangt.





