Pembrolizumab (Keytruda): Vorkommen fataler Hautreaktionen
Last Updated on May 11, 2017 by Joseph Gut – thasso
10. Mai 2017 – Swissmedic, das Schweizerische Heilmittelinstitut, informiert uns heute mittels eines “Dear Health Care Provider Letter” (DHPC), in Zusammenarbeit mit der Inhaberin der Marktzulassung, dass bei der Anwendung von Pembrolizumab (Keytruda) ein tödlicher Fall von Stevens-Johnson Syndrom (SJS) und ein tödlicher Fall von toxischer epidermaler Nekrolyse (TEN) aufgetreten sind.

In der Schweiz ist Pembrolizumab (Keytruda) als Monotherapie zugelassen a) zur Behandlung des fortgeschrittenen (nicht resezierbaren oder metastasierten) Melanoms bei Erwachsenen, und b) zur Zweitlinienbehandlung des fortgeschrittenen, metastasierten nicht- kleinzelligen Lungenkarzinoms (NSCLC) in genau definierten Situationen. Pembrolizumab (Keytruda) ist ein Immun-Checkpoint-Inhibitor, im Speziellen ein PD-1-Inhibitor,
Gemäss der Zulassungsinhaberin MSD Merck Sharp & Dohme AG (MSD) wurde kürzlich eine Überprüfung der Fälle von SJS und TEN durchgeführt, die mit Pembrolizumab (Keytruda) in klinischen Studien und nach Markteinführung berichtet wurden. Es gab 8 Fälle von SJS (6 in klinischen Studien und 2 nach Markteinführung) und 2 Fälle von TEN (beide nach Markteinführung). Alle berichteten Fälle waren schwerwiegend. Je ein Fall von SJS und TEN waren tödlich. Ungefähr 11‘000 Patienten wurden mit Pembrolizumab (Keytruda) in klinischen Studien behandelt und ungefähr 27‘000 Patienten nach Markteinführung. Nach Beurteilung der Gesamtheit der Daten und aufgrund des Schweregrads der Diagnose, ist MSD zum Schluss gekommen, dass ein möglicher Zusammenhang zwischen der Pembrolizumab (Keytruda) Therapie und dem Auftreten von SJS/TEN besteht.
Aufgrund dieser Überprüfung wird die Fachinformation von Pembrolizumab (Keytruda) gemäss den obenerwähnten Empfehlungen aufdatiert. Die jeweils aktuellste Fachinformation zu Pembrolizumab (Keytruda) wird auf “http://www.swissmedicinfo.ch” publiziert, und die aus dieser Mitteilung resultierenden Empfehlungen an die behandelnden Ärzte sind folgende:
- Beraten Sie die Patienten hinsichtlich der Risiken und des Nutzens von Pembrolizumab (Keytruda), einschliesslich der Risiken von SJS und TEN.
- Bei Anzeichen und Symptomen von SJS oder TEN setzen Sie Pembrolizumab (Keytruda) sofort aus und überweisen Sie den Patienten umgehend zur Abklärung und Behandlung an den Spezialisten.
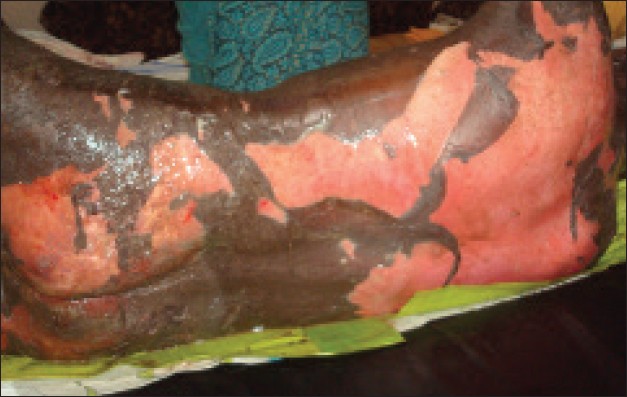
- TEN und SJS sind charakterisiert durch empfindliche erythematöse Flecken, die sich zu Blasen und Hautablösungen entwickeln. Typisch ist eine Mitbeteiligung der Schleimhäute. Der Hautmanifestation geht oft eine Phase mit Photophobie, Infektionssymptomen und Fieber voraus.
- Setzen Sie Pembrolizumab (Keytruda) dauerhaft ab, wenn SJS oder TEN bei einem Patienten bestätigt wird.
Im Zeitalter der theragenomischen und personalisiertrn Medizin wäre es nun sehr interessant und hilfreich zu wissen, ob die betroffenen Patienten Träger genetischer Prädispositionen für das Auftreten dieser schwerwiegenden Formen von SJS und TEN waren. Es ist bekannt, dass Patienten, welche Träger des HLA-B*5701 Alleles sind, z.B. mit Abacavir (Ziagen) nicht behandelt werden dürfen, da sie unweigerlich SJS und TEN, darunter fatale Fälle, entwickeln. Ebenso sind Patienten welche aus China, Südost-Asien und Indien stammen gehäuft Träger des HLA-B*1502 Alleles, welches für ein erhöhtes SJS- und TEN-Risiko nach Behandlung dieser Patienten mit einer Reihe von Arzneimitteln, z.B. Carbamazepin (Tegretol), verantwortlich ist. Sowohl als behandelter Arzt wie auch als Patient/Patientin würde man von einer modernen DHPC-Mitteilung erwarten, dass sie solche vitale Information enthält, welche im vorliegenden Falle zur prospektiven Identifikation von Patienten / Patientinnen mit hohem Risiko für SJS und TEN nach Behandlung mit Pembrolizumab (Keytruda) beitragen könnte.






